Noticias
null Nuevos modelos 'in vitro' con microesferas y nanopartículas
Fuente: La Verdad
Fundación Séneca respalda un proyecto de fertilidad basado en la tecnología celular y molecular, para estudiar la interacción entre el ovocito y el espermatozoide.
Las técnicas de reproducción asistida forman parte, desde hace ya algunos años, de la historia reproductiva de muchas parejas. Desde su introducción en la década de los 80, estas han mejorado considerablemente para lograr grandes avances en las técnicas de fecundación in vitro, sobre todo en la especie humana, pero no tanto para sacar a la luz las causas de la infertilidad. Según la Organización Mundial de la Salud (OMS), una de cada cuatro parejas en países en desarrollo se ha visto afectada por la infertilidad y se espera que esta incidencia aumente principalmente debido a que la maternidad se pospone para lograr objetivos profesionales y personales, o por factores como toxinas o la contaminación que están disminuyendo la calidad del esperma cada año. La importancia de las tecnologías de reproducción asistida (TRA) también se da en campos como la ganadería y la protección de especies en peligro de extinción, entre otros.
Este avance ha sido posible gracias a la Fundación Séneca -Agencia de Ciencia y Tecnología de la Región de Murcia, dependiente de la Consejería de Empresa, Empleo, Universidades y Portavocía-, dentro de la convocatoria 'Ayudas a la realización de proyectos para el desarrollo de investigación científica y técnica por grupos competitivos 2018', que termina en septiembre de este año, con un importe concedido de 46.160 euros.
La evolución de estas técnicas de reproducción asistida va hacia sistemas que sean capaces de reproducir y recrear las condiciones naturales que ocurren en el interior de un organismo, con entornos que mimeticen el espacio de fecundación y la mínima manipulación de gametos y embriones. Para todo esto, es primordial conocer el proceso de fecundación, mecanismo celular esencial de la reproducción sexual de mamíferos, un proceso altamente sincronizado durante el cual dos células germinales haploides, el óvulo y espermatozoide, se unen para producir una sola célula, embrión (cigoto). Conocer y describir las proteínas responsables del proceso de fecundación es fundamental para poder diseñar las dianas que generen nuevos avances en el campo de la reproducción, tanto a nivel de posibles deficiencias relacionadas con infertilidad, estrategias de control de poblaciones mediante métodos anticonceptivos o marcadores de calidad de los gametos, entre otros.
En este escenario, los componentes del grupo de investigación 'Gametogénesis, fecundación y desarrollo embrionario temprano' de la Universidad de Murcia y el IMIB, y con la colaboración de la doctora Enrica Bianchi del Cell Surface Signalling Laboratory (Wellcome Sanger Institute, Cambridge, UK), pusieron en marcha el proyecto 'Uso de microesferas y nanopartículas para el desarrollo de nuevos ensayos en reproducción', con el objetivo de desarrollar modelos 'in vitro' basados en la tecnología celular y molecular junto con la aplicación de microesferas y nanopartículas para el estudio de la interacción entre el ovocito y espermatozoide. En el desarrollo del proyecto también han colaborado la doctora Raquel Romar Andrés y el doctor Francisco García Vázquez, profesores e investigadores del Departamento de Fisiología de la Facultad de Veterinaria de la Universidad de Murcia. 
«Las investigaciones que hemos llevado a cabo durante los últimos 15 años y los diferentes laboratorios que hemos visitado nos han dado una visión bastante completa de los diferentes retos que tiene la investigación en el campo de la reproducción, donde los progresos son bastante lentos. La unión entre dos células tan especializadas, el óvulo y el espermatozoide, supone un abordaje muy específico que no se puede extrapolar de otros procesos biológicos. La investigación en reproducción necesita modelos específicos de estudio que permitan desentramar los mecanismos moleculares responsables de función para poder avanzar en sus aplicaciones, como son las técnicas de reproducción asistida», señala María Jiménez Movilla, profesora titular del Departamento de Biología Celular e Histología de la Facultad de Medicina de la UMU e investigadora del IMIB. El grupo de investigación lleva muchos años desarrollando proyectos basados en el estudio de los procesos moleculares y fisiológicos relacionados con la biología de la reproducción en mamíferos.
Limitaciones y soluciones
El equipo analizó que la investigación básica en el campo de la reproducción tiene muchas limitaciones. Por ejemplo, la recuperación de gametos y su uso en la investigación tiene implicaciones bioéticas y no está permitido en todas las especies. El uso de gametos o embriones humanos en la investigación está prohibido en la mayoría de los países, o los proyectos deben superar las estrictas evaluaciones de los comités de ética. Además, los estudios de gametos o embriones en otras especies de mamíferos implican el sacrificio o la intervención quirúrgica. La directiva europea 2010/63 / UE se refiere al Principio de Reemplazo, Reducción y Refinamiento (3R), por el cual el uso de animales con fines de investigación debe ser sustituído cuando sea posible, utilizando el mínimo número de animales. Por otro lado, según detalla María Jiménez, los estudios bioquímicos para la caracterización de la actividad de las proteínas implicadas conllevan la necesidad de una alta cantidad de muestras que en el caso del estudio del óvulo es muy complicado de abordar. Por lo tanto, se deben desarrollar nuevas estrategias para superar estas limitaciones.
«A nivel de investigación aplicada y tras años de investigación en Biología y Tecnología de la reproducción en mamíferos hemos detectado que uno de los principales problemas en las TRAs ha sido la manipulación de gametos y embriones durante las diferentes etapas del proceso, ya que éstos requieren condiciones de máximo control para preservar su habilidad fecundante y un desarrollo embrionario de calidad. Procesos tales como la maduración 'in vitro' de ovocitos, la fecundación 'in vitro', el cultivo embrionario y su desarrollo o la vitrificación requieren de la manipulación constante de ovocitos y embriones. Actualmente, esta manipulación requiere de un contacto físico directo que puede reducir la eficiencia de la tecnología aplicada o incluso causar pérdidas genéticas de un valor incalculable. Esta constante manipulación interfiere en los resultados finales y, por tanto, en la eficiencia de las técnicas de reproducción asistida», afirma. 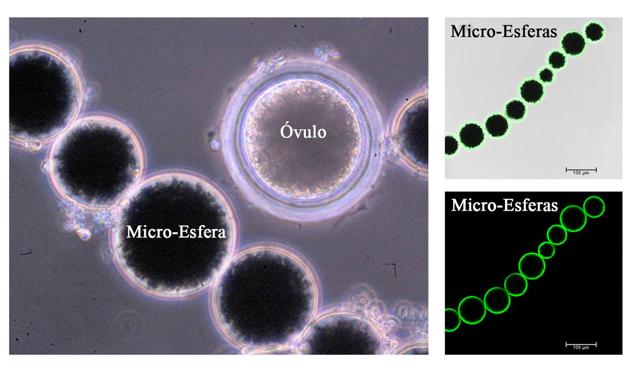
Ante esto, se propone el desarrollo de dos nuevos modelos para el estudio del proceso de fecundación y estudiar y analizar las posibles aplicaciones en las técnicas de reproducción asistida, con modelos 'in vitro' basados en la tecnología celular y molecular junto con la aplicación de microesferas y nanopartículas. En el primer caso, proponen un modelo en 3D que imite la forma del ovocito. Este modelo se obtendrá combinando microesferas magnéticas con las proteínas recombinantes del óvulo involucradas en la interacción y fecundación de gametos, como es la proteína ZP2, responsable del reconocimiento con el espermatozoide y la proteína Juno, receptora de la membrana plasmática del ovocito y responsable de la unión entre el espermatozoide y el óvulo. El desarrollo de un modelo 3D permitirá el análisis del papel de estas proteínas en diferentes especies de mamíferos puesto que la tecnología recombinante hace que este modelo sea fácilmente transferible a muchas especies. Además, reducirá el uso de gametos femeninos en ensayos 'in vitro' y podría implementarse en el sector la industrial para la selección 'in vitro' y técnica de evaluación de calidad de espermatozoides potencialmente fértiles.
En segundo lugar, proponen una nueva metodología de reproducción asistida que permitirá manipular ovocitos y embriones sin contacto físico. Para ello desarrollarán nanopartículas férricas especialmente diseñadas para unirse con la parte externa del ovocito y el embrión. «Una vez que nuestras nanopartículas se encuentren adheridas al óvulo o el embrión, éstos podrán moverse hacia cualquier dirección requerida o permanecer fijos evitando desplazamientos, todo esto sin una manipulación directa sino mediante la aplicación de un campo magnético. Esta nueva tecnología hará que el manejo de ovocitos y embriones sea más fácil que nunca, abriendo una nueva gama de aplicaciones», detalla.
El diseño de dos modelos se debe a que los dos comprenden la misma base molecular (uso de proteínas recombinantes conjugadas a microesferas o nanopartículas), pero con aproximación diferente a nivel biológico, por lo que el esfuerzo tecnológico será el mismo y de esta manera aumentan las posibilidades de éxito del objetivo general.
«La obtención de modelos 'in vitro' para el estudio de la interacción de gametos puede tener un fuerte impacto en el desarrollo de tecnología para la transferencia al sector industrial, tanto en empresas relacionadas con las clínicas de fecundación para la implantación de test de calidad de gametos, como para la utilización de éstos como base para el estudio de moléculas y su incorporación en los medios de fecundación», afirma la investigadora, quien añade que el difícil acceso a los gametos y su regulación ética hace que los modelos 'in vitro' presenten elevadas ventajas a la hora de realizar diferentes ensayos tanto en investigación básica como aplicada.
«Consideramos que el desarrollo de estos dos nuevos abordajes podría ser fundamental para avanzar en el conocimiento del proceso molecular que define el reconocimiento entre el espermatozoide y el óvulo, pero además tendrá una enorme aplicación en diferentes estrategias asociadas con la biotecnología de la reproducción», añade.
Validación
El modelo de microesferas ya ha sido desarrollado y validado para su utilización y se ha reflejado en diversas revistas científicas, además de haberse presentado los resultados en numerosos congresos científicos internacionales. En estos momentos están probando el modelo en otras especies. En cuanto al modelo de nanoesferas, el equipo investigador ha centrado sus esfuerzos en la transferencia al sector industrial para probar que el sistema es totalmente válido y aplicable a las técnicas de reproducción 'in vitro', teniendo como resultado que la metodología es totalmente inocua. María Jiménez afirma que «en el caso de las nanoesferas, esperamos que esta metodología pueda ser aplicada en técnicas de reproducción asistida y estamos llevando a cabo los pasos necesarios para generar una 'startup' que nos permita su comercialización», añade.
«El respaldo de la Fundación Séneca ha sido fundamental para poder llevar a cabo estas ideas, que han partido de hipótesis y hemos podido validar gracias a la financiación de este proyecto. A partir de estos resultados nuestro grupo ha sido beneficiario de una proyecto del Ministerio a nivel nacional y el desarrollo de proyectos relacionados con la transferencia y Prueba de concepto a nivel industrial», concluye con satisfacción la investigadora.