La estructura tridimensional de
una proteina es un factor determinante en su actividad biológica. Tiene un carácter
jerarquizado, es decir, implica unos niveles de complejidad creciente que dan lugar a 4
tipos de estructuras: primaria, secundaria, terciaria y cuaternaria. Cada uno de estos niveles se construye a partir del anterior.
La ESTRUCTURA PRIMARIA esta representada por la sucesión lineal
de aminoácidos que forman la cadena peptídica y por lo tanto indica qué aminoácidos
componen la cadena y el orden en que se encuentran. El ordenamiento de los aminoácidos en
cada cadena peptídica, no es arbitrario sino que obedece a un plan predeterminado en el
ADN.
Esta estructura define la
especificidad de cada proteina.

La ESTRUCTURA SECUNDARIA está representada por la disposición
espacial que adopta la cadena peptídica (estructura primaria) a medida que se sintetiza
en los ribosomas. Es debida a los giros y plegamientos que sufre como consecuencia de la
capacidad de rotación del carbono  y de la formación de enlaces débiles (puentes de
hidrógeno). y de la formación de enlaces débiles (puentes de
hidrógeno).
Las formas que
pueden adoptar son:
a) Disposición
espacial estable determina formas en espiral (configuración 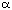 -helicoidal y las hélices de
colágeno) -helicoidal y las hélices de
colágeno)
 

Las  -hélice aparecen en rojo. -hélice aparecen en rojo.
b) Formas
plegadas (configuración  o de hoja plegada). o de hoja plegada).





c) También
existen secuencias en el polipéptido que no alcanzan una estructura secundaria bien
definida y se dice que forman enroscamientos aleatorios. Por ejemplo, ver en las figuras
anteriores los lazos que unen entre sí 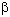 -hojas plegadas. -hojas plegadas.
La ESTRUCTURA TERCIARIA esta representada por los
superplegamientos y enrrollamientos de la estructura secundaria, constituyendo formas
tridimensionales geométricas muy complicadas que se mantienen por enlaces fuertes
(puentes disulfuro entre dos cisteinas) y otros débiles (puentes de hidrógeno; fuerzas
de Van der Waals; interacciones iónicas e interacciones hidrofóbicas).

Desde el punto de
vista funcional, esta estructura es la más importante pues, al alcanzarla es cuando la
mayoría de las proteinas adquieren su actividad biológica o función.
Muchas proteínas
tienen estructura terciaria globular caracterizadas por ser solubles en
disoluciones acuosas, como la mioglobina o muchos enzimas.

Sin embargo, no
todas las proteinas llegan a formar estructuras terciarias. En estos casos mantienen su
estructura secundaria alargada dando lugar a las llamadas proteinas filamentosas, que son insolubles en agua y
disoluciones salinas siendo por ello idóneas para realizar funciones esqueléticas. Entre
ellas, las más conocidas son el colágeno de los huesos y del tejido conjuntivo; la  -queratina del
pelo, plumas, uńas, cuernos, etc...; la fibroina del hilo de seda y de las telarańas y
la elastina del tejido conjuntivo, que forma una red deformable por la tensión. -queratina del
pelo, plumas, uńas, cuernos, etc...; la fibroina del hilo de seda y de las telarańas y
la elastina del tejido conjuntivo, que forma una red deformable por la tensión.
La ESTRUCTURA CUATERNARIA está representada por el acoplamiento de
varias cadenas polipeptídicas, iguales o diferentes, con estructuras terciarias
(protómeros) que quedan autoensambladas por enlaces débiles, no covalentes. Esta
estructura no la poseen, tampoco, todas las proteinas. Algunas que sí la presentan son:
la hemoglobina y los enzimas alostéricos.

 . .
|

